一起来学地质学(五)
发布日期:2025-01-23 09:59第二章 矿物
第一节矿物的概念
一、矿物的定义
矿物(mineral)是由地质作用形成的,在正常情况下呈结晶质的元素或无机化合物固体(Nickel,1995),是组成岩石和矿石的基本单元。那些由人工合成的产物,如人造水晶、人造金刚石等,虽然它们具有与矿物相同的特征,但它们不是地质作用形成的,故不称矿物。水、气体不是晶体,也不是矿物,冰则是矿物。煤不是无机化合物固体,不属于矿物。花岗岩虽是固体,但它是由长石、石英、黑云母多种物质聚集而成的,故不能称矿物。
准矿物(mineraloid)在产出状态、成因和化学组成等方面均具有与矿物相同的特征,但不是具有结晶构造的均匀固体。自然界为数很少,较常见者是A型蛋白石和水铝英石。
二、晶体、非晶质体与准晶体
晶体(crystal)是其内部原子或离子在三维空间呈周期性平移重复排列的固态物质。与晶体定义相对应,原子或离子在三维空间呈周期性平移重复排列的固体称为结晶质(crystalline)颗粒,简称晶质。习惯上,晶体是指具有几何多面体外形的晶体,而将不具几何多面体外形的晶体称为晶粒(crystalline grain)。
非晶质体(non-crystal)是其内部的原子或离子在三维空间不呈规律性重复排列的固体。与非晶质体概念相对应的物质是非晶质。
晶体是由结晶质构成的固体,因此,除个别特例以外,矿物均属于晶体。其内部原子、离子或分子呈有序排列的状态,称为晶体结构(crystal structure)。不同的晶体,因其内部原子、离子或分子的种类和排列方式的不同,故具有不同的晶体结构。
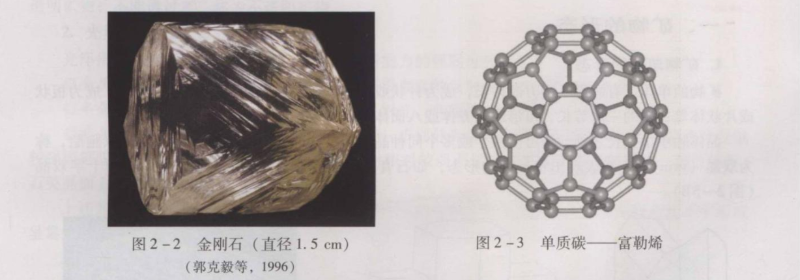
相同化学成分的物质在不同的环境条件(温度、压力等)下可以形成不同的晶体结构,从而成为不同的矿物,这种现象称为同质多象(polymorphism)。如碳原子在中、低级变质条件下呈石墨(graphite)出现,而在超高压条件下则变为金刚石(diamond)(图2-2)。两者成分相同但物理性质大不相同:金刚石是无色透明的最硬矿物,石墨是黑色不透明的极软矿物。
1985年发现的单质碳——富勒烯(C₆0),则是由60个碳原子构成的稳定分子,形似足球(图2-3),故又名足球烯。富勒烯在室温下为紫红色固态晶体(半导体),掺杂后可变成临界温度很高的超导体。2004年又发现石墨烯[即只有一个碳原子厚(厚0.335 nm)的单层石墨],打破了二维晶体无法真实存在的理论预言,从而发现了世界上最强、最硬、最韧、最薄且导电、导热性能特好的新型材料。这两个发现,在1996年和2010年分别获得物理学诺贝尔奖。我国青年学者CaoYuan等2018年发现石墨烯中非规超导电性(能量传送零损耗):只要将两层石墨烯旋转到1.1°的角度叠加,就可零阻力传导电子。石墨烯具有广泛的应用前景,如用于增强金属特性,作为超导体与新型催化剂,制造光学材料、太空电梯、超级计算机等。
此外,矿物晶体结构中的某种原子或离子可以部分地被性质相似的他种原子或离子替代而不破坏其晶体结构,此种现象称为类质同象(isomorphism)。如橄榄石((Mg,Fe)₂[SiO₄])中的Mg²+与Fe²+就呈类质同象的替代关系。矿物的化学式中凡写在同一圆括弧内并用逗号隔开的元素都具有此种关系。
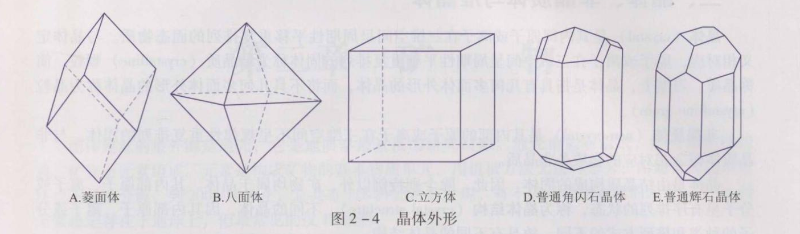
晶体因为内部原子、离子或分子排列规则,故在有足够生长空间的情况下它们能长成规则的几何多面体外形。包围晶体的平面称晶面(crystal face)。几何多面体的晶体外形就是其格子构造在宏观上的反映。如白云石(MgCa[CO₃]₂)常呈菱面体(rhombohedron)(图2-4A),磁铁矿(Fe₃O₄)常呈八面体(octahedron)(图2-4B),石盐(NaCl)常呈立方体(cube)(图2-4C),三者分别由6个菱形的晶面、8个等边三角形的晶面、6个正方形的晶面构成。多数矿物晶体是由几种不同形状和大小的晶面聚合而成的,如普通角闪石、普通辉石(图2-4D,E)。
由于受到自由生长空间的限制,多数晶体晶面发育不完整,或完全没有晶面,从而形成外形不规则的晶粒(晶体)。晶粒大小不一,较粗的用肉眼或放大镜就可以看出来者,称为显晶质;若晶粒细微,要通过显微镜才能加以分辨者,则称为隐晶质。
非晶质体是由非晶质构成的。由火山喷发出来的部分物质因冷凝极快,来不及结晶,则形成非晶质体,称之为火山玻璃;若条件变化,非晶质体可向晶质体转化。
准晶体(quasicrystal)发现于1984年,是一种新的凝聚态固体(罗谷风等,1985),其内部的原子或离子既不像非晶质体那样完全无序分布,又不像晶体那样呈三维周期性平移有序排列。准晶体的粒径一般只达微米级。目前尚未发现天然产出的(由地质作用形成的)准晶体(罗谷风等,1993)。
摘自《普通地质学》(第四版),舒良树主编。